الكيمياء الجدول الدوري
العناصر الكيميائية في الجدول الدوري مصنفة ضمن أعمدة تبين الخصائص المشتركة بينها. يكشف هذا التصنيف عن التركيب الذري، حيث تدور الإلكترونات حول النواة في مسارات ثابتة، وهذا يسهم في فهم التفاعلات الكيميائية والظواهر الفيزيائية مثل الأشعة الفوق البنفسجية والسينية.
يُعد الجدول الدوري أداة أساسية في الكيمياء لدراسة البنية الإلكترونية للعناصر وخصائصها الكيميائية. أصبح رمزًا بارزًا في العلم، موفرًا طريقة لفهم كيفية تجميع الذرات والجزيئات لتكوين المواد المختلفة.
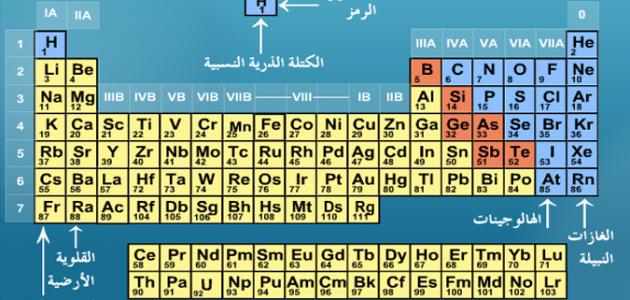
الفكرة التي قام عليها الجدول الدوري
قام العالمان، الروسي ماندليف والألماني ماير، بتصنيف العناصر مرتبة حسب زيادة العدد الذري من اليسار إلى اليمين.
العدد الذري يعبر عن عدد البروتونات الموجودة داخل نواة العنصر.
يتطابق عدد البروتونات مع عدد الإلكترونات في الذرة نفسها.
وزن الذرة، أو ما يعرف بعدد الكتلة، يحسب بجمع عدد البروتونات والنيترونات الموجودة فيها.
خلال مائة عام منذ أن طور ماندليف جدوله الدوري في عام 1869، شهدت الجداول الدورية تحديثات بلغت نحو 700 إصدار مختلف.
اليوم، يضم الجدول الدوري 118 عنصرًا.
العناصر مرتبة ضمن صفوف وأعمدة تجمعها خصائص فيزيائية وكيميائية مشتركة.
في أقصى الطرف الأيسر من الجدول، تقع المجموعة 1 وتشمل فلزات، بينما توجد اللافلزات في الطرف الأيمن، وبينهما تقع أشباه الفلزات.
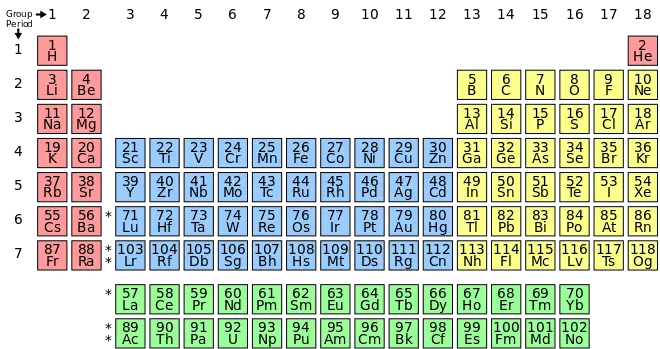
أسماء عناصر الجدول الدوري الــ 118 بالعربي
تتضمن العناصر الكيميائية من الهيدروجين الذي يحمل الرمز H، إلى الهيليوم الذي يُرمز له بـ He، ثم الليثيوم (Li) والبيريليوم (Be). تليهم العناصر بورون (B)، كربون (C)، نيتروجين (N)، أكسجين (O)، فلور (F) ونيون (Ne). كما يوجد الصوديوم (Na)، الماغنسيوم (Mg)، والألومنيوم (Al)، بالإضافة إلى السيليكون (Si)، الفوسفور (P)، الكبريت (S)، الكلور (Cl) والأرجون (Ar). فيما يتعلق بالمجموعات الأكثر ثقلاً، نجد البوتاسيوم (K) والكالسيوم (Ca) متبوعين بالسكانديوم (Sc)، التيتانيوم (Ti)، الفانديوم (V)، الكروم (Cr)، المنجنيز (Mn) والحديد (Fe).
تنضم إلى القائمة عناصر مثل الكوبالت (Co)، نيكل (Ni)، نحاس (Cu)، الزنك (Zn)، الجاليوم (Ga)، الجيرمانيوم (Ge)، الزرنيخ (As)، السيلينيوم (Se)، البروم (Br) والكربتون (Kr). كذلك نجد الروبيديوم (Rb)، السترونتيوم (Sr)، الإتريوم (Y)، والزركونيوم (Zr). العناصر مثل النيوبيوم (Nb)، الموليبدينيوم (Mo)، التكنيتيوم (Tc)، الروثينيوم (Ru)، الروديوم (Rh) والپالاديوم (Pd) تضيف تنوعاً كبيراً للقائمة.
الفضة (Ag)، الكادميوم (Cd)، الإنديوم (In)، والقصدير (Sn) هي أمثلة أخرى، إلى جانب الأنتيمون (Sb)، التيلوريوم (Te)، اليود (I) والزينون (Xe). السيزيوم (Cs) وعناصر اللانثانيد مثل اللانثانوم (La) والسيريوم (Ce) تليها عناصر مثل البراسيوديميوم (Pr) والنيوديميوم (Nd). العناصر الأثقل والنادرة مثل البروميثيوم (Pm) والساماريوم (Sm)، اليوروبيوم (Eu) والگادولينيوم (Gd)، تقدم تنوعاً في الخصائص والاستخدامات.
عناصر مثل الثوليوم (Tm)، الإتيربيوم (Yb)، اللوتيتيوم (Lu)، الهافنيوم (Hf) والتانتالوم (Ta) معروفة أيضاً في قائمة العناصر. الزئبق (Hg)، الثاليوم (Tl) والرصاص (Pb) مع غيرها من العناصر الثقيلة كالبزموث (Bi) والثوريوم (Th) جزء من هذه السلسلة الطويلة. أما العناصر الاصطناعية النادرة مثل البروتكتينيوم (Pa) واليورانيوم (U)، فهي تدل على تقدم العلم في هذا المجال. العناصر الفائقة الثقل مثل اللورنسيوم (Lr) والرذرفورديوم (Rf)، جنباً إلى جنب مع الدبنيوم (Db) والسيبورجيوم (Sg) تبرز التوسع الحديث في هذا الجدول الدوري.
تُختتم القائمة بعناصر مثل البوريوم (Bh)، الهاسيوم (Hs) والمايتنريوم (Mt)، وتظهر كيف أن العلم لا يتوقف عند حد معين بل يستمر في اكتشاف ودراسة عناصر جديدة، آخذة في الاعتبار التقدم المستمر في البحث العلمي.
هيكل الجدول الدوري للعناصر
يُنظم الجدول الدوري العناصر الكيميائية في صفوف تعرف بالدورات وأعمدة تُسمى المجموعات، حيث تشترك العناصر في أحد الصفوف بخصائص معيّنة كما تشترك تلك الواقعة في نفس العمود بصفات مشابهة أيضًا. يُقدم كل مربع في الجدول الدوري بيانات مهمة ومحددة عن عنصر معين، ومن هذه المعلومات:
– رمز العنصر: يتألف من حرف أو حرفين ويعبر عن الاسم الإنجليزي أو اللاتيني القديم للعنصر، مثلاً، الرمز (Ag) يُشير إلى الاسم اللاتيني “Argentum” والذي يعني الفضة.
– العدد الذري: يشير إلى كمية البروتونات الموجودة في نواة الذرة الواحدة وهو يُعد معياراً لتمييز العناصر عن بعضها البعض، حيث أن تغييرات في الإلكترونات أو النيترونات لا تؤثر على تحديد العنصر.
– الكتلة الذرية: تُمثل القيمة المتوسطة لكتل نظائر العنصر المختلفة.
– اسم العنصر: يظهر أحيانًا إلى جانب الرمز في الجداول الدورية، لتسهيل تعرف الدارسين على العناصر.
ما هي أهم عناصر الجدول الدوري؟ وما خصائصهم؟
تتميز الفلزات بتواجد ثلاثة إلكترونات أو أقل في غلافها الخارجي، وتضم معادن كالصوديوم والمغنيسيوم والألمنيوم. هذه المعادن تسهل عملية فقدان الإلكترونات من محيطها الإلكتروني ما يجعلها تحمل شحنات موجبة وتعمل كموصلات جيدة للكهرباء.
في المقابل، اللافلزات تحوي محيطاً خارجياً أكثر اكتمالاً بحيث يتعدى نصف السعة الإلكترونية، مثل الفسفور والأكسجين والكلور. هذه العناصر تتسم بخواص ترفض التيار الكهربائي نظراً لصعوبة إزاحة إلكتروناتها، وعادةً ما تكتسب إلكترونات لتصبح ذات شحنات سالبة.
أشباه الفلزات تشبه الفلزات في مظهرها لكنها تشغل منزلة وسط بين الفلزات واللافلزات من حيث الخواص. هذه العناصر تؤدي دوراً هاماً في الصناعات الكهربائية والإلكترونية مثل تصنيع الترانزستورات.
الغازات الخاملة، التي تم الكشف عنها في أواخر القرن التاسع عشر، تضم الهيليوم والنيون وغيرها. هذه الغازات لا تتفاعل كيميائياً تقريباً وقد استمدت أهميتها من فصلها الصعب واكتشافات غيرت فهمنا للعلم الحديث، مثل تحديد وزن الأرجون الذي واجه صعوبات عدة قبل أن يُعلن.
أما النظائر فهي أشكال مختلفة لذات العنصر تختلف بالكتلة لكن تظل في الموقع ذاته في الجدول الدوري. على سبيل المثال، القصدير لديه عشر نظائر بينما يمتلك الكربون ثلاثة. استكشاف النظائر كان له دور بالغ في توسيع معرفتنا بتكوين العناصر وإضافة العديد من العناصر الجديدة إلى قائمة المعروفة.

